▲台灣新藥人體實驗年逾300件,十大死因之首「癌症」最多。(圖/示意圖/達志影像)
記者嚴云岑/台北報導
對於某些罕見疾病及癌患,參加新藥的臨床試驗可能是他們的最後希望。根據食藥署統計,每年受理的藥品實驗計畫正逐漸增加,2015年總共受理302件,其中222件為多國同時進行,80件為單獨於國內進行,其中又以受試項目又以癌症43.4%佔最大宗。
食藥署簡任技正蔡士智表示,2004年台灣推出臨床實驗計畫時,申請案件僅有119件,因應國人飲食習慣改變與高齡化社會來臨,2015年受理件數已升至302件。其中又以國人十大死因之首「惡性腫瘤」131件佔大宗,其次為B肝、C肝、愛滋病、茲卡病毒等感染疾病38件,第三名則為失智症、癲癇等神經與精神性疾病。
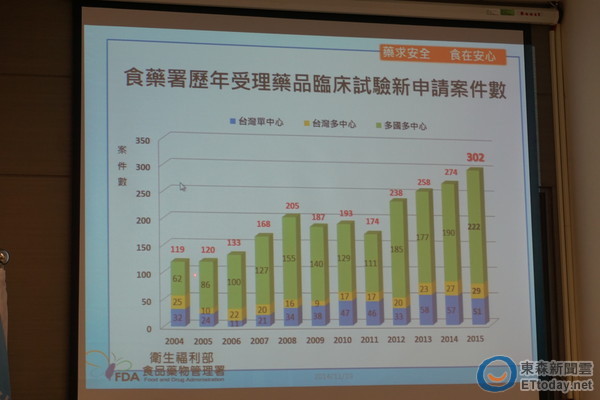
▲食藥署新藥臨床試驗有逐年上升的趨勢。(圖/記者嚴云岑攝)
為了讓臨床試驗資訊公開透明化,國際間已有不少臨床試驗資料庫公開藥品試驗訊息,其中美國國家衛生研究院營運的ClinicalTrials.gov網站規模最大,可檢索全世界正在進行的國際多中心臨床試驗,我國也自2006年起,建置了「台灣藥品臨床試驗資訊網」,供病患參考。
在食藥署「台灣藥品臨床試驗資訊網」中,不僅可查詢到試驗計畫名稱、試驗藥品、試驗目的、試驗階段、宣稱適應症,試驗醫院、試驗委託單位、試驗執行狀態及試驗聯絡人資訊也包含在內。

▲食藥署簡技蔡士智說,臨床試驗的特性兼具科學、嚴謹。(圖/記者嚴云岑攝)
蔡士智建議,使用該網站可先由「名詞解釋」、「認識臨床試驗」開始瀏覽,瞭解參與臨床試驗受試者的權利、義務及應注意事項等基本觀念,個人在參加臨床試驗前,也應向主持醫師充分詢問相關問題,包括試驗目的、過程、可能的風險及副作用及損害補償機制等,經審慎評估後再簽署同意書。
根據食藥署統計,近3年來共有1~2件參與臨床實驗後因療效未達預期,或者認為醫院對其照顧不周而申訴的案例。蔡士智說臨床試驗是自願參與,受試者可隨時退出,其醫療照顧不會受到影響。若真的有問題,可向各大醫院的人體倫理委員會或食藥署、試驗委託者提出申訴,保障自身權益。
▼食藥署參與臨床試驗宣導手冊。(圖/記者嚴云岑攝)



讀者迴響